ISRIB 발견부터 임상연구 연대기
피터 월터 교수의 연구실에서 시작된 ISRIB(Integrated Stress Response Inhibitor)의 개발사는 단순한 약물 발견을 넘어, 세포가 스트레스를 관리하는 근본적인 방식에 대한 이해를 재정립한 획기적인 사건으로 기록된다. 2013년 UCSF에서 발견된 이 작은 분자는 기존의 '스트레스 반응 억제는 위험하다'는 독성학적 통념을 뒤집고, 단백질 번역 조절이 인지 기능과 신경 퇴행성 질환 치료의 핵심 열쇠가 될 수 있음을 증명해 냈다. 본 연혁은 ISRIB가 처음 발견된 순간부터, 그 분자적 기전이 규명되고, 전임상 모델에서의 효능이 입증되어, 마침내 인간을 대상으로 한 임상 시험에 이르기까지의 연혁을 상세히 기록한다. 추후에 일어나는 사건은 다른 사람들에 의해 추가되길 바란다.
연표
2010
[고속대량스크리닝(HTS) 수행]
[ 고속대량스크리닝(HTS) 수행]
2010부터 2012년 동안 고속대량스크리닝(HTS)을 수행하였다. 그리하여 ATF4 리포터를 이용해 10만 개 화합물 중 ISRIB를 식별하였다.
당시 연구팀은 소포체(ER) 스트레스 반응, 특히 PERK(Protein Kinase RNA-like Endoplasmic Reticulum Kinase) 경로를 조절할 수 있는 저분자 화합물을 찾고 있었다. 이들은 106,281개의 화합물 라이브러리를 스크리닝하기 위해 정교한 리포터 시스템을 구축했다. 이 시스템은 ATF4(Activating Transcription Factor 4)의 번역 조절 부위를 반딧불이 루시퍼라아제 유전자와 결합한 것으로, 세포에 스트레스를 주면 빛을 내도록 설계되었다. 세포에 thapsigargin이라는 약물을 처리하여 강력한 소포체 스트레스를 유발한 뒤, 루시퍼라아제의 발현(즉, 스트레스 반응)을 억제하는 화합물을 탐색했다. 그 결과, 수십만 개의 후보 물질 중에서 독보적인 효능을 보인 화합물이 발견되었다. 연구팀은 이 물질에 ISRIB(Integrated Stress Response InhiBitor)라는 이름을 붙였다. (thapsigargin을 처리하면 소포체 내 단백질은 misfold하게 되어 소포체 내에 구조를 잡지 못한 단백질이 축적하게 되어 소포체에 스트레스가 발생하게 된다.)
2013
[ISRIB 발견 eLife 논문 발표]
2013년, Carmela Sidrauski박사와 피터 월터 교수는 eLife에 획기적인 발견을 발표했다.
1. 나노몰 단위의 효능과 입체 특이성: ISRIB는 세포 실험에서 5nM의 IC50(반수 억제 농도)을 보일 정도로 매우 강력했다. 가 세포 내의 특정 단백질 포켓에 열쇠와 자물쇠처럼 정확하게 결합한다는 것을 시사했다.
2. 하위 단계 작용: 가장 흥미로운 점은 ISRIB가 eIF2 α 를 인산화 시키는 상위효소(PERK 등)를 억제하지 않는다는 것이다.
3. 기억력 향상 효과: 이 논문의 하이라이트는 동물 행동 실험이었다. ISRIB를 투여받은 쥐들은 모리스 수중 미로)와 공포 조건화 실험에서 대조군보다 월등히 뛰어난 공간 기억력과 공포 기억력을 보였다.
Pharmacological brake-release of mRNA translation enhances cognitive memory (2013) Carmela Sidrauski Diego Acosta-AlvearArkady KhoutorskyPunitha VedanthamBrian R HearnHan LiKarine GamacheCiara M GallagherKenny K-H AngChris WilsonVoytek OkreglakAvi AshkenaziByron HannKarim NaderMichelle R ArkinAdam R RensloNahum SonenbergPeter Walter elife https://doi.org/10.7554/eLife.00498
2014
[피터 월터, 레스커 상 수상]
이 발견은 학계에 큰 충격을 주었다. 기존에는 스트레스 반응을 억제하면 세포가 방어 기제를 잃어 독성에 취약해질 것이라 예상했으나, ISRIB 처리 세포들은 생존에 문제가 없었을 뿐만 아니라 오히려 기능이 향상되었기 때문이다. 이는 피터 월터 교수가 2014년 권위 있는 앨버트 래스커 기초 의학 연구상(Albert Lasker Basic Medical Research Award)을 수상하는 데 기여한 핵심 연구 중 하나가 되었다.
2015
[Calico와의 라이선스 계약]
2015년, 구글(Alphabet)이 설립한 노화 연구 기업 칼리코(Calico Life Sciences)는 UCSF와 독점 라이선스 계약을 체결했다. 이 계약은 피터 월터 연구실의 ISR 조절 기술에 대한 권리를 포함했으며, ISRIB를 발견한 주역인 카멜라 시드라우스키 박사가 칼리코로 자리를 옮겨 임상 개발을 주도하게 되었다. 이는 기초 과학의 발견자가 직접 상용화를 이끄는 이상적인 모델을 보여주었다.
칼리코는 글로벌 제약사 애브비(AbbVie)와 협력하여 "ABBV-CLS-7262(성분명: Fosigotifator)"라는 임상 후보 물질을 도출했다. 이 약물은 ISRIB와 화학적 구조는 다르지만, eIF2B를 안정화시켜 활성을 높이는 기전은 동일하다. 특히 뇌혈관장벽(BBB) 투과성이 우수하고 경구 투여가 가능하도록 설계되었다.
[ISRIB 기전 규명]
2015년, 월터 연구팀은 ISRIB의 표적이 eIF2B임을 명확히 했다. 생화학적 실험을 통해 ISRIB가 eIF2B 복합체(complex)를 이량체화(dimerization)시켜 안정화함으로써 효소 활성을 높인다는 구체적인 작동 원리를 밝혔다. 즉, ISRIB가 '분자 접착제(molecular staple)'처럼 작용하여 eIF2B를 활성화된 형태로 묶어준다는 사실을 제시했다.
The small molecule ISRIB reverses the effects of eIF2α phosphorylation on translation and stress granule assembly (2015) Carmela Sidrauski Anna M McGeachyNicholas T IngoliaPeter Walter eLife https://doi.org/10.7554/eLife.05033
2017
[외상성 뇌손상 (TBI) 치료]
PNAS에 발표된 연구에서 수잔나 로시(Susanna Rosi) 교수와 월터 교수는 ISRIB가 외상성 뇌손상(TBI) 후유증을 치료할 수 있음을 보였다. TBI를 입은 쥐들은 부상 후 몇 달이 지나도 심각한 학습 및 기억 장애를 겪으며, 해마에서 ISR이 만성적으로 활성화되어 있었다. 놀랍게도, 부상 후 수주가 지난 시점에 ISRIB를 투여했음에도 불구하고, 쥐들의 인지 기능이 정상 수준으로 완전히 회복되었다. 이는 뇌 손상으로 인한 인지 장애가 영구적인 세포 사멸 때문만이 아니라, 가역적인 대사 차단 상태일 수 있음을 시사했다.
Inhibition of the integrated stress response reverses cognitive deficits after traumatic brain injury (2017) Austin Chou, Karen Krukowski, Timothy Jopson, Ping Jun Zhu, Mauro Costa-Mattioli, Peter Walter and Susanna Rosi Proc Natl Acad Sci U S A 114(31):E6420-E6426. doi: 10.1073/pnas.1707661114.
2018
[cryo–EM을 이용한 구조 규명]
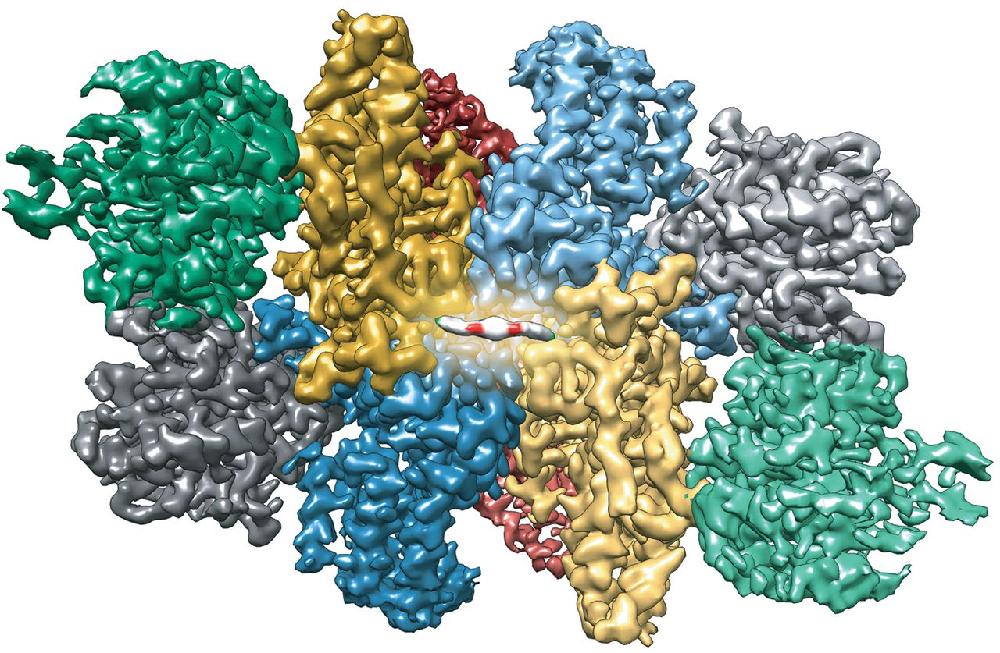
2018년 3월 피터 월터 박사의 Science 지에 발표된 연구는 ISRIB 개발의 정점을 찍었다. 연구팀은 초저온 전자현미경(Cryo-EM) 기술을 이용하여 ISRIB가 결합된 인간 eIF2B 복합체의 원자 단위 구조를 규명하는 데 성공했다.
Structure of the nucleotide exchange factor eIF2B reveals mechanism of memory-enhancing molecule (2018) Jordan C. Tsai, Lakshmi E. Miller-Vedam, Aditya A. Anand, Priyadarshini Jaishankar, Henry C. Nguyen, Adam R. Renslo, Adam Frost, and Peter Walter Science 356(6383) DOI: 10.1126/science.aaq09
[공격성 전립선암의 사멸]
Science Translational Medicine에 발표된 연구는 신경계 질환이 아닌 암 치료에서의 가능성을 제시했다. 공격적인 전립선암 세포들은 생존을 위해 ISR을 이용해 단백질 합성을 부분적으로 억제하는 전략을 사용한다. 연구팀이 ISRIB를 처리하여 이 '브레이크'를 강제로 해제하자, 암세포들은 통제 불능의 단백질 과잉 생산 상태에 빠져 사멸했다. 이는 ISRIB가 맥락에 따라 세포를 보호할 수도(신경세포), 죽일 수도(암세포) 있음을 보여주는 정밀 의학의 예시였다.
Development of a stress response therapy targeting aggressive prostate cancer (2018) Nguyen HG, Conn CS, Kye Y, Xue L, Forester CM, Cowan JE, Hsieh AC, Cunningham JT, Truillet C, Tameire F, Evans MJ, Evans CP, Yang JC, Hann B, Koumenis C, Walter P, Carroll PR, Ruggero D. Sci Transl Med. 10(439):eaar2036. doi: 10.1126/scitranslmed.aar2036.
2019
[다운 증후군 인지 기능 회복]
Science에 게재된 논문에서 연구팀은 다운 증후군 모델 생쥐(Ts65Dn)의 뇌에서도 ISR이 비정상적으로 활성화되어 있음을 발견했다. 이로 인해 장기 기억 형성에 필수적인 단백질 합성이 저해되고 있었다. ISRIB 투여는 억제성 시냅스 전달을 정상화하고 시냅스 가소성을 회복시켜, 다운 증후군 쥐들의 기억력을 야생형 쥐 수준으로 끌어올렸다.
Activation of the ISR mediates the behavioral and neurophysiological abnormalities in Down syndrome (2019) Ping Jun Zhu, Sanjeev Khatiwada, Ya Cui, Lucas C Reineke, Sean W Dooling, Jean J Kim, Wei Li, Peter Walter, Mauro Costa-Mattioli Science. 366(6467):843-849. doi: 10.1126/science.aaw5185.
[새로운 eIF2B 활성제를 개발]
데날리 테라퓨틱스(Denali Therapeutics)가 DNL343을 eIF2B 활성제로 개발하여 공식적인 임상 개발 단계로 진입시킨 시점은 2019년 말에서 2020년 초다. 2019년 12월 초에 데날리는 DNL343에 대한 임상시험계획승인(CTA) 신청서를 제출했다. 이것이 DNL343이 연구 단계를 넘어 공식적인 '임상 개발' 단계로 진입한 시점이다. 그리고 2020년 1월에는 제38회 J.P. 모건 헬스케어 컨퍼런스에서 DNL343 프로그램을 대외적으로 공식 발표하고, 1월 중 CTA 승인을 받아 건강한 지원자를 대상으로 한 임상 1상을 시작할 계획임을 알렸다.
DNL343은 데날리 테라퓨틱스가 자체적으로 발굴한 물질이다. 이 물질은 루게릭병(ALS)과 같은 신경퇴행성 질환에서 나타나는 통합 스트레스 반응(ISR)을 억제하기 위해 개발되었다.
2020
[노화 역행]
가장 대중적인 관심을 끈 연구는 2020년 12월 eLife에 발표된 노화 관련 연구였다. 연구팀은 늙은 쥐(19개월 령, 인간의 65세 상당)에게 단 3일간 ISRIB를 투여했다. 그 결과, 늙은 쥐들의 공간 기억력과 작업 기억력이 젊은 쥐 수준으로 '회춘'했다. 또한 해마의 뉴런 활성도가 재설정되고, 노화와 관련된 염증 반응(인터페론 반응 등)이 감소했다. 이 연구는 노화로 인한 인지 저하가 하드웨어의 영구적 손상이 아니라, 소프트웨어(신호 전달 체계)의 오류일 수 있으며, 약물로 이를 재부팅(reboot)할 수 있다는 희망적인 메시지를 던졌다.
2021
[백질 소실병 임상 1상 시험]
2021년 1상 시험이 시작되었고, 2023년 4월 첫 환자 투약이 이루어졌다. 2024년 6월에는 미 FDA가 이 약물을 희귀질환 치료제 개발 가속화 프로그램인 START(Support for clinical Trials Advancing Rare disease Therapeutics) 파일럿 프로그램 대상으로 선정했다. 이는 규제 기관이 이 기전의 과학적 타당성을 높이 평가하고 있음을 보여준다. 임상은 2027년까지 진행될 예정이다.
가장 먼저 시작된 임상 시험 중 하나는 백질 소실병(Vanishing White Matter Disease, VWMD) 환자를 대상으로 한 것이었다(NCT05757141). VWMD는 eIF2B 유전자의 돌연변이로 인해 발생하는 희귀 유전 질환으로, 환자들은 만성적인 ISR 활성화로 인해 뇌의 백질이 녹아내리는 증상을 겪는다.
질병의 원인이 eIF2B의 불안정성이므로, eIF2B를 물리적으로 안정화시키는 '스테이플' 약물은 가장 직접적인 치료제가 될 수 있다는 가정으로 시작된 것이다.
2023
[근위축성 측삭 경화증]
가장 큰 기대를 모았던 것은 루게릭병으로 알려진 ALS에 대한 임상 시험(HEALEY ALS Platform Trial - Regimen F)이었다. ALS 환자의 신경세포에서는 TDP-43 단백질 응집체가 발견되며, 이것이 ISR을 유발하여 신경세포 사멸을 초래한다고 알려져 있다.
2023년 시작된 이 임상은 Fosigotifator의 효능을 평가하기 위해 설계되었다. 2025년 1월 발표된 탑라인 결과에 따르면, Fosigotifator는 불행히도 1차 평가지표(ALSFRS-R 점수로 측정한 질병 진행 지연)를 충족하지 못했다.
비록 주 목표 달성에는 실패했지만, 고용량 투여군에서 근력 및 호흡 기능 저하가 둔화되는 긍정적인 신호가 포착되었다. 또한 약물은 매우 안전했으며 내약성이 우수한 것으로 확인되었다. 이는 동물 모델의 결과를 인간의 복잡한 퇴행성 질환에 적용하는 것이 얼마나 어려운지를 보여주는 사례임과 동시에, 특정 하위 그룹이나 용량 조절을 통해 가능성이 남아있음을 시사한다.
2024
[주요 우울 장애로의 확장]
흥미롭게도 신경퇴행성 질환에서의 고전에도 불구하고, 개발사들은 정신 질환으로 적응증을 확장하고 있다. 2024년 말, 주요 우울 장애(MDD) 환자를 대상으로 Fosigotifator의 안전성과 효능을 평가하는 임상 시험(NCT06618118)이 시작되었다. 이는 만성 스트레스와 우울증이 뇌의 단백질 합성 저하와 연관되어 있다는 가설에 기반한 것으로, ISR 조절제의 새로운 활로가 될 수 있겠다.
[DNL343에 관한 논문 발표]
데날리 측은 2024년에 의약화학 저널(Journal of Medicinal Chemistry)을 통해 DNL343의 구체적인 발굴 과정과 화학적 구조 최적화 과정에 대한 논문을 발표하기도 했다.
Discovery of DNL343: a potent, selective, and brain-penetrant eIF2B activator designed for the treatment of neurodegenerative diseases (2024) Robert A Craig 2nd, Javier De Vicente, Anthony A Estrada, Jianwen A Feng, Katrina W Lexa, Mark J Canet, William E Dowdle, Rebecca I Erickson, Brittany N Flores, Patrick C G Haddick, Lesley A Kane, Joseph W Lewcock, Nathan J Moerke, Suresh B Poda, Zachary Sweeney, Ryan H Takahashi, Vincent Tong, Jing Wang, Ernie Yulyaningsih, Hilda Solanoy, Kimberly Scearce-Levie, Pascal E Sanchez, Liwei Tang, Musheng Xu, Rui Zhang, Maksim Osipov J Med Chem 67(7):5758-5782.
doi: 10.1021/acs.jmedchem.3c02422.2025
[새로운 단백질인 FTL1 규명]
2025년 8월, UCSF 연구진은 노화된 뇌의 인지 기능 저하와 관련된 새로운 단백질인 FTL1을 규명했다. 비록 ISRIB와 직접적인 기전은 다를 수 있으나, 이는 UCSF와 월터 교수의 후예들이 여전히 '노화의 가역성'을 증명하기 위해 분자적 타겟을 발굴하고 있음을 보여준다. FTL1의 조절이 ISRIB와 같은 스트레스 반응 조절제와 결합될 때 어떤 시너지를 낼 수 있을지는 향후 중요한 연구 주제가 될 것이다.
Targeting iron-associated protein Ftl1 in the brain of old mice improves age-related cognitive impairment (2025) Laura Remesal, Juliana Sucharov-Costa, Yuting Wu, Karishma J. B. Pratt, Gregor Bieri, Amber Philp, Mason Phan, Turan Aghayev, Charles W. White III, Elizabeth G. Wheatley, Bende Zou, Brandon R. Desousa, Julien Couthouis, Isha H. Jian, Xinmin S. Xie, Yi Lu, Jason C. Maynard, Alma L. Burlingame & Saul A. Villeda Nature Aging volume 5, pages 1957–1969

